砹
性质
砹具有极高的放射性。所有砹同位素的半衰期都在12小时以下,并会衰变成铋、钋、氡以及其他砹同位素。在首101种化学元素中,只有钫的稳定性比砹低。
人们对砹的宏观特性所知甚少。 其寿命太短,因此可用于研究的量极为有限。 可观量的砹元素会释放大量辐射,将自身加热,迅速气化。 砹一般归为非金属或类金属。 有科学家认为,砹能够形成凝聚态金属物质。
物理
砹的大部分物理特性都是根据理论或实验证据推算而得的。 例如,卤素的原子量越高,色泽就越深(氟几乎无色,氯呈亮绿色,溴呈棕色,而碘呈深灰或紫色)。如果该趋势持续,那么砹将会具有黑色金属质地。 根据类似的趋势,可推断砹的熔点和沸点比轻卤素都要高,估值分别为575K和610 K。 然而一些实验证据显示,砹的熔点和沸点有可能比理论预测的低。 砹的升华作用比碘缓慢,其蒸气压也较低。 在室温下把砹置于玻璃表面,1小时之后一半的砹会气化。
固体砹的晶体结构目前是未知的, 对于砹是否会形成双原子分子(At 2 ),目前也未有证据证实或否定。 某些文献主张At 2 从未被观测到,因此并不存在; 另一些文献则表示或暗示它是存在的。 尽管争议持续,但是砹双原子分子的许多属性都有理论的预测值, 如密度为6.2至6.5 g/cm 。
化学
砹的许多化学属性都是通过在极稀释的砹溶液中用放射性示踪剂进行研究得出的。 大部分属性,例如负离子的形成等,都与其他卤素相符。 它也同时拥有一些金属的特性,比如会电镀到阴极上, 在氢氯酸中与金属的硫化物共沉淀, 以及会在强酸中形成正离子。
砹在鲍林标度上的电负性为2.2,比碘的2.66低,与氢相同。但是砹化氢(HAt)的负电荷预计更靠向氢原子, 且砹在阿莱﹣罗周标度(Allred-Rochow scale)上的电负性为1.9,比氢的2.2低,所以可能应更准确地称其为“氢化砹”。
化合物
砹的化学活性比碘低,因此是卤素中活性最低的元素。 科学家成功合成了多种砹化合物,量极少。这些化合物会因砹的放射性而迅速瓦解,因此研究机会非常宝贵。实验一般把稀释砹溶液混合在大量的碘溶液中。碘作为载体,可保证有足够的量进行化学分析,如过滤和沉淀等。

砹化氢的空间填充模型
早期研究砹化学的科学家已发现,砹可以和氢形成砹化氢。 砹在(稀释)硝酸中会轻易氧化、酸化,形成At 或At 。加入银(I)会使小部分砹沉淀出来,形成砹化银(I)(AgAt)。相比之下,碘则不会被氧化,且会沉淀为碘化银(I)。
已知的金属砹化物很少, 其中包括钯、银和铅的砹化物。利用推算的方法可以得出砹化银以及各种碱金属和碱土金属的砹化物的属性。
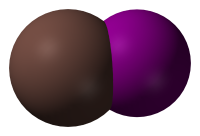
一碘化砹是已知最重的互卤化物。
在气体状态下,砹会与其他卤素碘、溴和氯反应,形成双原子互卤化物,如AtI、AtBr和AtCl。 Atl和AtBr可在水中产生:砹与碘/碘离子溶液反应形成AtI,砹与碘/一溴化碘/溴离子溶液反应形成AtBr。过量碘离子或溴离子会导致产生 AtBr − 2 和 AtI − 2 离子; 在氯离子溶液中,反应会与氯离子达致平衡,产生 AtCl − 2 或 AtBrCl 。 在硝酸溶液中用重铬酸氧化砹元素,加入氯离子会产生一种分子,可能是AtCl或AtOCl。用类似的方法可以产生 AtOCl − 2 或 AtCl − 2 。 在利用等离子离子源的质谱仪中,将其他卤素的气体加入到含有砹且充满氦气的空间中,会分别产生[AtI] 、[AtBr] 和[AtCl] 。这有助证明砹在等离子离子态下可以形成稳定的中性分子。 人们尚未发现砹的任何氟化物。科学家猜测,这是因为这种化合物反应性极强,可能在形成后瞬间与容器玻璃壁反应产生不挥发的物质。 虽然氟化砹有可能能够形成,但实验需要用到液态卤素氟化物。
砹在高氯酸溶液中与某些氧化剂(例如溴和过硫酸钠)反应,会产生AtO 、 AtO − 2 和AtO 。 在氢氧化钾溶液中,次氯酸钾能把砹氧化,形成 AtO − 3 。 用二氟化氙(在热碱性溶液中)或高碘酸(在中性或碱性溶液中)再次进行氧化,可产生高砹酸离子 AtO − 4 。不过,这种离子只有在中性或碱性溶液中才会稳定。 在酸性溶液中,一价砹会和碘酸银(I)和重铬酸铊(I)等不可溶金属盐共沉淀。有科学家因此认为,砹能够以正离子的形式与含氧负离子(如碘酸和重铬酸离子等)形成盐。
砹可以和其他氧族元素成键,如和硫形成S 7 At 、 At(CSN) − 2 ,和硒形成硒脲配合物,以及和碲形成砹﹣碲胶体。 另外,砹在适当条件下,还会与氮、 铅 和硼 键合。
已知的有机砹化合物包括四砹化碳(CAt 4 )。 砹可以替换苯中的一个氢原子,形成C 6 H 5 At,氯可以再将其氧化为C 6 H 5 AtCl 2 。该化合物在碱性次氯酸盐溶液中会转化为C 6 H 5 AtO 2 。
历史

门捷列夫1871年的元素表,其中碘以下的位置为空格
1869年德米特里·门捷列夫所发表的元素周期表中,碘以下的位置为空格。在尼尔斯·玻尔确立了化学元素分类的物理基础后,确定第五个卤素应该在碘以下。在正式发现之前,这一元素被称为eka-碘(eka在梵文中意为“一”),就是“碘之下一格”的意思。 多人尝试在自然中寻找该元素,但由于其含量极为稀少,许多人的发现都是错误的。
美国阿拉巴马理工学院(今奥本大学)的弗雷德·艾利森(Fred Allison)等人在1931年首次声称发现85号元素。他们将该元素命名为“alabamine”,符号Ab,以纪念学院所在地阿拉巴马州。科学界在其后的几年中都使用这一名称。 然而在1934年,伯克利加州大学的H·G·麦克弗森(H. G. MacPherson)推翻了艾利森的实验方法的有效性。 1937年,英属印度达卡(今孟加拉达卡市)的化学家拉真达拉·德(Rajendralal De)也同样错误发现85号元素。他将其命名为“dakin”,并表示它是钍衰变系中与镭F(即钋-210)对等的核素。他的报告中关于这一元素的数据并不符合砹的属性,而至今dakin究竟是什么仍不得而知。

砹的发现者之一埃米利奥·塞格雷
1940年,瑞士化学家瓦尔特·敏德(Walter Minder)宣布在镭A(即钋-218)的β衰变产物中发现第85号元素,并以瑞士的拉丁文名称“ Helvetia ”将该元素命名为“helvetium”。不过,贝尔塔·卡尔利克(Berta Karlik)和特罗德·贝尔奈(Traude Bernert)无法重现实验的结果,因此推论敏德实验所用的氡气受到了污染(氡-222是钋-218的母同位素)。 1942年,敏德与英国科学家爱丽丝·雷-史密斯(Alice Leigh-Smith)合作,宣布在钍A(即钋-216)的β衰变产物中发现85号元素的另一同位素。他们将其命名为“anglo-helvetium”,其中的“anglo”是英国的意思。 卡尔利克和贝尔奈同样无法重现这一结果。
1940年,戴尔·科尔森(Dale R. Corson)、肯尼斯·罗斯·麦肯西(Kenneth Ross MacKenzie)和埃米利奥·塞格雷终于在伯克利加州大学成功分离出该元素。他们并没有在自然界中寻找,而是在回旋加速器中对铋-209进行α粒子撞击来合成砹元素(释放两个中子后形成砹-211)。 产物迅速进行放射性衰变,因此发现团队将其取名为“astatine”,词源为希腊文中的“ἄστατος”(ástatos,意为“不稳定”)。 三年后,卡尔利克和贝尔奈在自然产生的衰变链中发现了砹元素。 此后科学家在一共四个自然衰变链中的三个当中发现了砹。
同位素
砹共有32种已知同位素,原子量为191和193至223。 砹没有稳定或长寿命的同位素。
砹共有23种同核异构体,也就是某同位素的一个或多个核子处于激发态时的原子核。同核异构体也可称为亚稳态,也就是其内部能量比基态能量高,容易衰变回基态。每种同位素可以拥有多个同核异构体。最稳定的砹同核异构体是砹-202m1, 半衰期约为3分钟;最为不稳定的是砹-214m1,半衰期只有265纳秒。
砹的α衰变能量符合重元素的规律。 较轻的砹同位素拥有较高的α衰变能量,而能量随原子核质量的增加而降低。砹-211的能量却比它前面的同位素高出许多,因为其原子核有126个中子──126是一个幻数,即中子壳层都已填满。虽然砹-211的半衰期与砹-210的相近,但是砹-211的α衰变概率有41.81%,比砹-210的0.18%高出许多。 接着的两种同位素则释放更多能量。砹-213释放的能量是所有砹同位素中最高的,所以它也是寿命最短的同位素。 尽管较重的同位素释放较少能量,但是由于β衰变(电子发射)概率也随着提升,所以所有砹同位素都是不稳定的。 早在1950年,科学家就预测砹不拥有任何β稳定的同位素(即不进行β衰变的同位素)。 实验证明,除了砹-213、214、215和216m以外,所有砹同位素都可进行β衰变。 砹-210及以下同位素进行β 衰变(正子发射),砹-216及以上同位素进行β 衰变,砹-212可同时进行这两种衰变模式,砹-211则进行中子捕获。
最稳定的砹同位素是砹-210,半衰期为8.1小时。该同位素的主要通过β 衰变形成寿命较长(相对其他砹同位素而言)的钋-210。一共只有5种砹同位素的半衰期超过1小时(原子量从207到211)。基态最不稳定的同位素是砹-213,半衰期为125纳秒。这一同位素会经α衰变形成近乎稳定的铋-209。
自然存量

镎衰变系:镎-237延续下来,中间经过砹-217
砹是自然界中最稀有的非超铀元素,在地壳中每一时刻只有不到1克的总量。 所有在地球形成时存在的砹元素都早已衰变殆尽了,而今天自然中的砹都是重元素的衰变产物。砹曾经被认为是地球上最稀有的元素,但科学家之后发现高浓度含铀矿藏里含有经中子捕获产生的超铀元素锫,而锫比砹更稀有。
自然产生的砹同位素共有6种(砹-214至砹-219)。 它们的半衰期都很短,所以都只以痕量存在。 没有数据显示砹能在恒星中形成。
其中四种自然同位素(砹-215、217、218和219)是在自然衰变链中发现的。钫-223是砹-219的母同位素,其α衰变概率只有0.006%,所以就算和其他砹同位素相比,砹-219同样极为稀有。然而它的半衰期却是所有自然砹同位素中最长的(56秒)。 砹-219会衰变成钋-215,再经β衰变形成砹-215,概率只有0.00023%。南北美洲16公里深的地壳以内,每一时刻只有大约一兆(万亿)个砹-215原子。 砹-218是钋-218的β衰变产物,可在自然现。与钫-223和钋-215一样,形成砹的途径并不是主要的衰变途径。 不过,镎衰变系从镎-237开始,一直到钫-221都只有唯一的衰变途径,而钫-221也只会衰变成砹-217。
自然同位素镤-226、227和228会经三重α衰变产生砹-214、215和216。 但是这些同位素也都非常稀有,所以砹-214至216一般都不被当做是自然同位素。
合成
形成
砹的主要生产方法是用高能α粒子对铋-209进行撞击。每次的产量十分微少,现今的技术每一生产周期可以产出2太拉贝克勒尔(即2万亿贝克勒尔),约等于25微克。
砹-211是目前唯一一个具有商业用途的砹同位素。 首先把铋金属溅射到金、铜或铝表面上,每平方厘米约含50至100微克。这一铋层(或是氧化铋)再与铜片融合,从而制成核反应的铋目标体。 目标体在不易反应的氮气中存放, 并以水进行降温,以避免产生了的砹过早地挥发。 α粒子(氦-4原子核)在如回旋加速器等粒子加速器中 高速撞击铋目标。虽然使用的只有一种铋同位素(铋-209),但有三种可能发生的核反应,分别形成砹-209、210和211。通过把加速器的最高能量调整在砹-211和砹-210的所需能量之间,科学家能够选择性地生产砹-211,并避免其他同位素的形成。
分离
核反应过后所产生的砹与各种其他元素混杂,因此需要经过分离过程。 含有砹元素的铋目标体加热至270 °C,这可气化所有挥发性放射性同位素。之后温度提高至800 °C。虽然80%的砹会在此温度下气化,但铋也同时开始气化。 砹的气化过程在600 °C以下速率较慢,但在800 °C以上就会迅速从铋表面上挥发出来。 气体凝聚后在水冷铂表面上收集,再转移到U形石英器皿中。石英器皿再加温至130 °C,以移除杂质(一般是钋),然后到500 °C。这时气化了的砹可收集到指形冷凝器中。 这样得出的纯化砹可以用弱硝酸溶液洗出冷凝器,作化学和物理分析等用途。这种方法的砹产量可以达到30%。
应用及安全
砹-211具有核医学应用。 刚制成的砹需要马上使用,因为在7.2小时之后,其总量就会减半。砹-211会释放α粒子,或经电子捕获衰变成释放α粒子的钋-211,所以可用于α粒子靶向治疗。
砹和碘一样会积聚在甲状腺,但程度较低。如果释入全身循环,砹会以放射性胶体的形式累积在肝脏当中。 碘-131是另一种用于医学的放射性同位素。砹-211与它最大的医用分别在于,碘-131会释放高能β粒子,而砹-211则不会。β粒子的穿透能力比较重的α粒子强许多:砹-211所释放的α粒子可在周围组织穿透约70 µm,而碘-131所释放的β粒子则可穿透约2 mm,这是前者的30倍左右。 因此使用砹-211可以对甲状腺施以适量的放射性治疗,但同时不足以破坏邻近的副甲状腺组织。由于半衰期更短,穿透能力也较弱,所以砹一般比碘-131更加适合作放射性诊断。
然而,在老鼠和猴子身上进行的实验指出,砹对甲状腺的破坏比碘-131大得多。重复注射砹会造成腺体坏死和异型增生。这些实验也显示,砹可以对任何生物的甲状腺造成损坏。 早期研究还指出,注射致命量的砹还会使乳房组织的形态进行变化, 不过这一结论仍具争议。
参阅
辐射防护 ( 英语 : Radiation protection )
Ts
备注
^ 但是,如果砹置于金或铂表面上,则这一“半升华期”可以长达16小时。这可能是砹与贵金属间某种未知的交互作用所导致的。
^ 这也有可能只是吸附作用。
^ 根据阿莱﹣罗周标度所用的算法,氢的电负性其实会与氧的3.5相近,这并不合理。因此,氢的电负性需定义为2.2。
^ 碘会在水中与砹反应,但仍可以作为载体,因为这些反应所需的不但有I ,还有碘离子I 。
^ 使用三氟化氯对砹进行氟化所产生的物质粘附在玻璃的表面。然而反应却形成了一氟化氯、氯气和四氟化硅。 该实验进行后十年,理论预测该化合物确实不具挥发性。这与其他卤素的对应化合物属性相驳,但与氟化氡相似。
^ 表中的质量过剩以能量等量作单位;产物质量过剩是子同位素和α离子的质量过剩之和;α半衰期指忽略α以外的其他衰变模式后的半衰期。
^ 尚没有证据显示砹-221会进行α衰变,因此其衰变能量和能量过剩都不是测量而得的,而是经理论预测估算的。
^ “m1”指同位素位于基态以上的最低能量状态,“m2”指基态以上第二低能量状态,如此类推。如果只有一种亚稳态,可以省略数字,只写“m”,如砹-216m。
^ 这意味着如果忽略α以外的衰变模式,那么砹-210的α半衰期有4,628.6小时(128.9天),而砹-211只有17.2小时(0.7天)。因此砹-211的α衰变途径比砹-210不稳定得多。
^ 砹在较低温度会和铋形成不挥发的化合物,但这些化合物在700至800 °C时会分解。
书目
Kugler, H. K.; Keller, C. "At, Astatine", system no. 8a. Gmelin handbook of inorganic and organometallic chemistry 8 8th. Springer-Verlag. 1985. ISBN 3-540-93516-9.
Lavrukhina, A. K.; Pozdnyakov, A. A. Аналитическая химия технеция, прометия, астатина и франция [Analytical Chemistry of Technetium, Promethium, Astatine, and Francium]. Nauka. 1966 (俄文) .
Zuckerman, J. J.; Hagen, A. P. Inorganic Reactions and Methods, the Formation of Bonds to Halogens. John Wiley & Sons. 1989. ISBN 978-0-471-18656-4.
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

相关资料

- 有价值
- 一般般
- 没价值








24小时热门
推荐阅读
知识互答
关于我们

APP下载




























{{item.time}} {{item.replyListShow ? '收起' : '展开'}}评论 {{curReplyId == item.id ? '取消回复' : '回复'}}