硝酸
历史
硝酸和硫酸一样由公元8世纪阿拉伯炼金术士阿布·穆萨·贾比尔·伊本·哈扬(Jabir ibn Hayyan)在干馏绿矾和硝石混合物时发现,也是一种化学肥料。
自然存在
雷雨时能产生少量的硝酸。打雷时放出的能量让空气中的N 2 和O 2 发生反应,产生NO:
NO 2 和水反应产生硝酸和一氧化氮:
有些海鞘( Ciona intestinalis )也能分泌硝酸御敌 。
结构
硝酸是平面分子,其中心原子N原子为sp 杂化。由于羟基上的氢原子与另外一个氧原子形成了氢键,分子才呈平面结构,而且N的三根键长都不相同。N原子垂直于分子平面的一个p轨道是满的,它与未连接H的两个氧原子上的p轨道共轭,形成 Π Π --> 3 4 {\displaystyle \Pi _{3}^{4}} 大Π键。分子内氢键也是硝酸沸点较低的原因。
硝酸去掉一个氢原子的结构是 硝酸根 ,一般带一个负电荷(硝酸根离子)。硝酸根具有对称的平面等边三角形结构, 4个原子形成大 Π Π --> 4 6 {\displaystyle \Pi _{4}^{6}} 键,多出来的1个电子在离域Π键里。
硝酸去掉一个羟基的结构是 硝基 -NO 2 。硝基的正离子叫硝酰正离子。
物理性质
纯硝酸为无色、容易挥发的液体,沸点约为83 °C,凝固点约为-42 °C,密度为1.51g/ml。可以与水以任意比混溶。硝酸是二氧化氮溶于水生成的,但由于二氧化氮溶于水并不会完全水解成硝酸,会有少量的二氧化氮分子存在,因此硝酸水溶液呈淡黄色,也会挥发出棕红色的NO 2 。一般的浓硝酸指的是16mol/L的HNO 3 水溶液,密度为1.42g/ml。

发烟硝酸

70%硝酸
化学性质
纯硝酸可以发生自偶电离:2HNO 3 H 2 O+NO 2 +NO 3
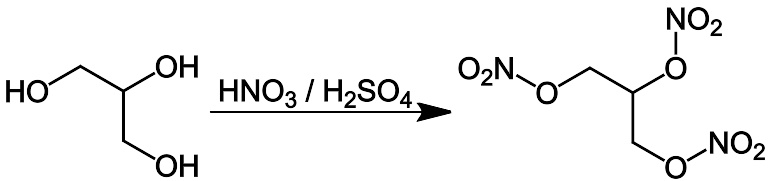
硝酸作为氮的最高价(+5)水化物,具有很强的酸性,一般情况下认为硝酸的水溶液是完全电离的。硝酸可以与醇发生酯化反应,如硝化甘油的制备。(实际上我们会使用浓硫酸,产生大量NO 2 ),成本较低而且较容易处理,与其他更强的脱水剂,例如P 4 O 10 ,也可以产生大量的硝酰阳离子,这是硝化反应能进行的本质。
硝酸的水溶液无论浓稀均具强氧化性及腐蚀性,溶液越浓其氧化性越强。硝酸在光照条件下分解成水、NO 2 和O 2 ,方程式如下:
因此硝酸一定要盛放在棕色瓶中,并置于阴凉处保存。硝酸能溶解许多种金属(可以溶解银),生成盐、水、氮氧化物。随着溶液浓度的减小,其还原产物逐渐由高价向低价过渡,从最浓到最稀可生成NO 2 、NO、N 2 O、N 2 、NH 4 NO 3 。还原产物一般是混合物,金属与浓硝酸反应多生成NO 2 ,与稀硝酸反应下生成如NO等较低价化合物。
铁、铝、铬等金属遇冷的浓硝酸可以发生钝化现象,只在表面形成一层致密的氧化膜,不会完全反应掉。
浓硝酸和浓盐酸的物质的量按1:3混合,即为王水,能溶解金、铂等稳定金属。
硝酸盐大多易遇热分解,生成氧气、氮氧化物、金属氧化物(也可能生成亚硝酸盐等)。
硝酸铵中的硝酸根与铵根,平均能量大于有其平均价数之一氧化二氮,在固态时发生均化反应(因为动力学原因,在溶液内不发生)(NH 4 NO 3 )即加热或撞击分解生成一氧化二氮和水,一般使用现代合成炸药引爆,威力与TNT相去不远,但成本极低。因此被用于国防工业及工程上而被誉为国防工业之母(主要制造硝基含能化合物(现代合成炸药)。硝酸钾就是黑火药的成分之一)。
制备
工业上用二氧化氮与水混合制备硝酸:奥士华法
4NH 3(g) +5O 2(g) →4NO (g) +6H 2 O (g) (铂铑催化)(ΔH=−905.2kJ)
2NO (g) +O 2(g) →2NO 2(g) (ΔH=−114kJ/mol)
3NO 2(g) +H 2 O (l) →2HNO 3(aq) +NO (g) (ΔH=−117kJ/mol)
总式:NH 3(g) +2O 2(g) →2NO (g) +2HNO 3(g) (铂铑催化)
反复把生成的气体通入水中,即可得到较纯的硝酸。其原料二氧化氮是由氨氧化而得,因此硝酸工业与制氨工业密不可分。
纯硝酸制备
制造纯硝酸则是把浓硫酸与硝酸盐混合加热,反应式为:
NaNO 3 +H 2 SO 4 →NaHSO 4 +HNO 3
工业用途
硝酸是在工业上和实验室中都很常用的一种酸。
作为硝酸盐和硝酸酯的必需原料,硝酸被用来制取一系列硝酸盐类氮肥,如硝酸铵、硝酸钾等;也用来制取硝酸酯类或含硝基的炸药,如三硝基甲苯(TNT)、硝化甘油。
由于它同时具有氧化性和酸性,硝酸也被用来精炼金属:即先把不纯的金属氧化成硝酸盐,排除杂质后再还原。
人体影响
硝酸不论浓稀溶液都有氧化性和腐蚀性,因此对人很危险,仅溅到皮肤上也会引起严重烧伤。皮肤接触硝酸后会慢慢变黄,最后变黄的表皮会起皮脱落(硝酸和蛋白质接触后,会导致黄蛋白反应而变性)。此外,浓硝酸需以深色玻璃瓶盛装,避免受到光照反应释出有毒的NO 2。
与金属的反应
一般的酸与活泼金属反应,生成氢气:
而硝酸与金属反应,不会生成氢气。 这是因为硝酸根(NO 3 )的氧化性比氢离子(H )强。
浓硝酸(约16mol/L)与金属反应,主要生成红棕色的二氧化氮气体:
稀硝酸(约6mol/L)与金属反应,主要生成一氧化氮气体:
更稀的硝酸(约2mol/L以下)与金属反应,产物从一氧化二氮到氮气到铵根离子不等。
普遍认为,硝酸与金属反应时,各还原产物(NO 2 、NO、N 2 O、N 2 、NH 3 )都可以生成。 但由于硝酸、水、氮氧化物、亚硝酸、连二次硝酸等物质间的多个平衡,不同浓度硝酸的还原产物有很大差异。
极稀硝酸和活泼金属生成氢气的说法,没有得到证实。
参看
硝酸盐
亚硝酸、连二次硝酸
镪水——硫酸、盐酸、硝酸
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

- 有价值
- 一般般
- 没价值








24小时热门
推荐阅读
知识互答
关于我们

APP下载


























{{item.time}} {{item.replyListShow ? '收起' : '展开'}}评论 {{curReplyId == item.id ? '取消回复' : '回复'}}